
Ernährungsstudien unterliegen nicht den Standards wie etwa Medizin. Dennoch ist die Ernährungsforschung auf dem Weg zu einer harten Wissenschaft.

Mit den Vorsätzen fürs neue Jahr ist es so eine Sache. Die andere Sache ist, dass für aber auch gegen alles, sich immer eine Studie finden lässt.
Wer kann an Studien teilnehmen? Denise Olbrich vom Lübecker Zentrum für klinische Studien über wissenschaftliche Standards, Hoffnungen und Risiken.

Es ist die erste bundesweite Studie dieser Art: Forscher wollen herausfinden, wie viele Deutsche eine Corona-Infektion schon überstanden haben.
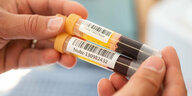
Medizinhistoriker, die Tests von Westmedikamenten in der DDR untersuchten, konnten die Vorwürfe entkräften, dass dort Menschenversuche stattfanden.

„Anwendungsbeobachtungen“ sind oft Scheinstudien, um den Umsatz von Medikamenten zu steigern. Dafür zahlt die Pharmaindustrie jährlich 100 Millionen Euro.
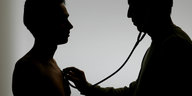
Die neue EU-Verordnung zu klinischen Studien regelt auch, wie die teilnehmenden Patienten über die Arzneimitteltests informiert werden müssen.

Die EU verpflichtet die Industrie zu mehr Transparenz bei klinischen Studien. Gegen die Macht der Medikamente-PR hilft das wenig, sagt Jörg Schaaber.
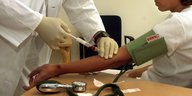
Die Veröffentlichung der Daten von klinischen Studien soll nach EU-Recht nun doch verpflichtend sein. Auch eine Genehmigung der Ethikkommission ist vorgesehen.
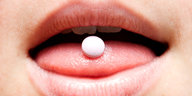
Sollen Ergebnisse klinischer Medikamentenstudien für alle zugänglich sein? Die EU will mehr Transparenz. Die Pharmaindustrie fürchtet um Geschäftsgeheimnisse.

Das Schutzniveau bei der EU-Richtlinie für Arzneiversuche mit Menschen reicht nicht aus, sagt die Bundesregierung. Sie fordert grundlegende Änderungen.
Die Pharmafirma GlaxoSmithKline unterstützt die Kampagne zur Offenlegung klinischer Studien. 2012 erhielt der Konzern noch eine Rekordstrafe.

