Arzneimitteltests mit Schutzbedürftigen: Vorab eine Blanko-Verfügung
Gesundheitsminister Gröhe (CDU) will, dass auch nicht einwilligungsfähige Demente als Versuchskaninchen für Pharmaversuche dienen können.

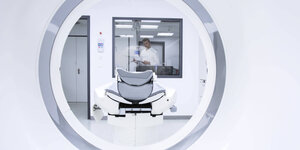
BewohnerInnen einer Wohngemeinschaft für Demenz-Kranke Foto: dpa
HAMBURG taz | Der Grundsatz gilt für jede Forschung mit Menschen: Wer an einer klinischen Studie teilnimmt, muss wissen können, worauf er sich einlässt. Zwingend ist eine verständliche Aufklärung über Forschungszwecke und mögliche gesundheitliche Risiken. Nur so ist – zumindest theoretisch – erreichbar, was Juristen „informierte Einwilligung“ nennen.
In der Praxis gibt es bereits Studienbereiche, die von dieser Regel bewusst abweichen. Das, gemessen an der Anzahl der Probanden, größte Beispiel ist der Biomaterialbanken- und Big-Data-Forschungsverbund namens Nationale Kohorte (Nako), gefördert mit über 200 Millionen Euro aus Steuergeldern.
Wer bei der Nako mitmacht, stellt Körperflüssigkeiten und Gesundheitsdaten für molekulargenetische Analysen und mögliche Forschungsprojekte zur Verfügung – ohne deren Inhalt und Verantwortliche zum Zeitpunkt der Einwilligung kennen zu können.
Im sensiblen Gebiet der Arzneimittelprüfungen steht nun die nächste rechtliche Aufweichung an. Betroffen wären Menschen, die als besonders schutzbedürftig gelten – weil sie so schwer erkrankt sind, dass sie nicht mehr in der Lage sind, die gebotene Aufklärung zu verstehen und einzuwilligen.
Geht es nach dem Willen der Bundesregierung, sollen künftig zum Beispiel demenziell veränderte Menschen an der Erprobung neuer pharmazeutischer Wirkstoffe teilnehmen, die ihnen gesundheitlich nichts nützen können. Über eine entsprechende Reform des Arzneimittelgesetzes (AMG) soll der Bundestag am 8. Juli entscheiden – trotz Protesten.
Ohne Nutzen für den Probanden
Die ersten, die Alarm schlugen, waren Repräsentanten der evangelischen und katholischen Kirche. Ihre Stellungnahme warnt davor, „dass der Mensch zum Nutzen anderer instrumentalisiert wird“. Empört hatte die Kirchenleute ein kurzer Passus im 60 Seiten dicken AMG-Reformentwurf. Demnach sollen erwachsene Menschen, „die nicht in der Lage sind, Wesen, Bedeutung und Tragweite der klinischen Prüfung zu erkennen“, trotzdem dabei mitwirken dürfen – auch wenn von vornherein klar ist, dass es keine gesundheitliche Besserung für den Probanden geben wird.
Vorausgesetzt wird gemäß Gesetzentwurf hingegen, dass die Studie das Potenzial hat, derjenigen Gruppe von Patienten zu nutzen, zu der nicht einwilligungsfähige Versuchspersonen gehören – und außerdem, dass Mitwirkende früher, als sie dies gesundheitlich noch konnten, mit einer „Patientenverfügung“ pauschal erklärt haben, dass sie sich bei Demenz oder neurodegenerativen Erkrankungen als Testperson zur Verfügung stellen wollen – für Arzneistudien, deren Rahmenbedingungen ihnen noch völlig unbekannt sind.
Es gibt keinen Grund zur Eile
Die AMG-Novelle soll offiziell deutsches Recht an die EU-Verordnung 536/2014 anpassen. Die nationalen Gesetzgeber haben allerdings Gestaltungsspielräume, und es gibt keinen Anlass zur Eile: Das neue EU-Recht gilt frühestens ab Oktober 2018.
Gegen die Regierungspläne opponieren erkennbar auch Unionsabgeordnete, allen voran der Ex-Behindertenbeauftragte Hubert Hüppe (CDU). Gemeinsam mit Abgeordneten aus anderen Fraktionen, etwa Ulla Schmidt (SPD), Kathrin Vogler (Linke) und Kordula Schulz-Asche (Grüne) sammelt CDU-Politiker Uwe Schummer im Parlament Unterschriften für einen Änderungsantrag, der im Wesentlichen dafür eintritt, die geltende Rechtslage zu bewahren.
SPD-Gesundheitsexperte Karl Lauterbach hat derweil einen „Kompromissvorschlag“ angekündigt, der „die Möglichkeit der Verwirklichung eines selbstbestimmten altruistischen Wunsches, Menschen mit der gleichen Erkrankung zu helfen“, schaffen soll. Der Vorschlag sehe vor, dass Menschen mit Demenz, die an gruppennützigen Arzneistudien teilnehmen sollen, diese Absicht noch im Vollbesitz ihrer geistigen Kräfte in einer Vorsorgevollmacht oder Betreuungsverfügung aufgeschrieben haben müssen.
Neues Konzept: Probanden-Verfügung
Tritt später tatsächlich Demenz auf, müsste der rechtliche Vertreter vor konkreten Forschungsvorhaben jeweils entscheiden, ob sein Schutzbefohlener hier wohl gern mitmachen würde oder nicht. Und der Parlamentarische Geschäftsführer der CDU/CSU-Fraktion, Michael Grosse-Brömer, hat eine weitere Variante in Aussicht gestellt: die „sogenannte Probanden-Verfügung“, verfasst irgendwann, nach vorheriger Aufklärung durch einen Arzt.
Logik, Ergebnis und Zweck der Pläne von Lauterbach und Grosse-Brömer unterscheiden sich im Kern kaum vom Entwurf der Regierung, die ja eine „Patientenverfügung“ als Instrument blanko erteilter Einwilligungen bevorzugt.
Abseits rechtlicher und taktischer Feinheiten haben die Abgeordneten bis zum 8. Juli kaum noch Zeit, angemessen der inhaltlichen Frage nachzugehen, ob und welcher Bedarf für gruppennützige Arzneistudien besteht. Der Vorstoß von Gesundheitsminister Hermann Gröhe (CDU), unterstützt vor allem von Forschungsministerin Johanna Wanka (CDU), ist nämlich auch in der medizinischen Fachwelt umstritten.
Der Mensch wird damit zum Nutzen anderer instrumentalisiert
Deutlich wurde das bei der Sachverständigen-Anhörung zur geplanten AMG-Reform. Als Hauptbefürworter gruppennütziger Arzneiprüfungen trat am 9. Mai im Gesundheitsausschuss Wolfgang Maier auf. Der Bonner Psychiatrieprofessor ist ein vielbeschäftigter Fachmann. So hat er auch die Entwicklung der im Januar 2016 vorgestellten „Leitlinie Demenzen“ koordiniert und für deren Methodenteil ein paar Hinweise zu möglichen Interessenkonflikten abgegeben. Laut Selbstdarstellung hat Maier auch mit den Firmen Schwabe Pharma, Lilly, Lundbeck und Pharma-consult kooperiert und von diesen Geld erhalten – wohl für Leistungen wie Vorträge und Beratungstätigkeiten; Details und die gezahlten Geldbeträge legte er aber nicht offen.
Vor dem Gesundheitsausschuss beklagte Maier „fehlende Therapiemöglichkeiten bei fortgeschrittener Demenz“ und erklärte in seiner schriftlichen Stellungnahme, wovon er Besserung erwartet: „Derzeit sind für die Alzheimer-Krankheit kausal ansetzende Wirkstoffe in Entwicklung, die in sehr frühen initialen Stadien der Demenzentwicklung krankheitsmodifizierend wirken (sog. ‚aktive Impfung‘) und so das Fortschreiten der Krankheit langfristig verzögern oder gar aufhalten können“, schrieb Maier. „Für den Erfolg solcher Wirkstoffe bestehen gute Chancen, wie Sekundäranalysen zu klinischen Studien zeigen.“
Gruppennützige klinische Studien
Sollten sich die Ergebnisse bestätigen, werde sich laut Maier „die Frage ergeben, ob diese Wirkstoffe auch in fortgeschrittenen Stadien der Demenz einen bremsenden oder symptomreduzierenden Effekt haben“. Um dies zu überprüfen, seien „gruppennützige klinische Studien (randomisiert und kontrolliert) notwendig“.
Anders argumentierte der Vorsitzende der Ethikkommission des Landes Berlin, Professor Martin Hildebrandt. Für ihn ist es „nicht nachvollziehbar, warum der Gesetzgeber einer Absenkung des Schutzniveaus für nicht einwilligungsfähige Personen zustimmen sollte“. Hildebrandt erklärte dazu: „Ein zwingendes medizinisch-wissenschaftliches Bedürfnis für placebokontrollierte klinische Prüfungen mit nicht einwilligungsfähigen Personen besteht aus meiner Sicht nicht.“ Die Behandlung von Patienten etwa mit Demenz vom Typ Alzheimer könne mit längst zugelassenen Arzneimitteln erfolgen. Entsprechendes gelte auch für die Behandlung eines Schlaganfalls, einer Sepsis oder eines Schocks.
Im Ergebnis ähnlich hat sich der Vertreter der Bundesärztekammer, Professor Hans-Werner Bothe, positioniert: „Aus Sicht der Bundesärztekammer“, so der Neurochirurg, „besteht zurzeit kein Grund, gruppennützige, fremdnützige Forschung zusätzlich zu fördern.“


Leser*innenkommentare
Mind
Ein solches Gesetz ist nicht hinnehmbar. Es gehört auch keinesfalls in die Rubrik Wissenschaft sondern in den Bereich Wirtschaft, da hier die chemische Industrie verdienen will.
Lesebrille
"... die ihnen gesundheitlich nichts nützen..." Das klingt so harmlos. Tatsächlich haben Medikamente aber auch Nebenwirkungen. Herr Gröhe sagte einmal dazu, dass es natürlich nur harmlose Nebenwirkungen sein dürften. Diese Aussage ist nicht nur unhaltbar, ich halte sie, gelinde gesagt, erst recht für einen Gesundheitsminister, für zu naiv!
Ein Medikament, dessen Wirkung noch nicht bekannt ist, soll Personen verabreicht werden, bei denen davon auszugehen ist, dass es nicht das einzige Medikament ist, das sie schlucken. Generelle Unverträglichkeiten und/oder auch Wechselwirkungen mit anderen Medikamenten: unbekannt. Folgen für die Menschen: unbekannt. Mögliche Mortalitätsrate durch Verabreichung: unbekannt.
Forciert und stark unterstützt wird das Projekt von einem Mann, sponsort by Pharmacy! Wow, das nenne ich nenne ich unabhängige Förderung...!
Dagegen protestieren übrigens nicht nur Kirchenfrauen und -männer und PolitikerInnen, sondern auch einzelne behinderte und kranke Menschen, sowie Vereine und Verbände. Beim Gedanken der (unfreiwilligen) Vernützlichung von Menschen wird nämlich vielen schlecht.
Hier werden Begehrlichkeiten geweckt, die Menschenrechte errodieren lassen - es kann jeden treffen!